- 工业上金属钡的制取包括氧化钡制取和金属热还原(铝热还原)制取金属钡两个步骤。
- (1)氧化钡的制取
- 优质重晶石矿首先需要经手选和浮选,之后经过去铁和硅后得到含硫酸钡大于96%的精矿。将粒度小于20目的矿粉与煤或石油焦粉按重量比4∶1混合,在反射炉内于1100℃下焙烧,硫酸钡被还原成硫化钡(俗称"黑灰"),用热水浸出得到的硫化钡溶液。为了使硫化钡转化成碳酸钡沉淀,需要向硫化钡水溶液中加入碳酸钠或通入二氧化碳。将碳酸钡与炭粉混合后于800℃以上煅烧,即可制得氧化钡。需要注意的是,氧化钡在500-700℃时氧化生成过氧化钡,在700-800℃时过氧化钡又可分解生成氧化钡,因而为了避免生产过氧化钡,煅烧产物需要在惰性气体保护下冷却或淬冷。
- (2)铝热还原法生产金属钡
- 铝还原氧化钡的反应因配料不同有以下两种:
- 6BaO+2Al→3BaO•Al2O3+3Ba↑
- 或:4BaO+2Al→BaO•Al2O3+3Ba↑
- 在1000~1200℃时,这两种反应产出的钡很少,所以需要用真空泵将钡蒸气不断地从反应区转移到冷凝区,反应才能不断向右进行。反应后的残渣有毒,需经处理才能弃去。
- (1)碳酸钡的制备方法
- ①碳化法
- 碳化法主要是将重晶石和煤按照一定比例混合,经破碎进入回转炉在1100-1200℃下焙烧还原制得硫化钡熔体。在硫化钡溶液中通入二氧化碳进行碳化,反应如下:
- BaS+CO2+H2O=BaCO3+H2S
- 将得到的碳酸钡浆液经脱硫洗涤和真空过滤,然后在300℃下进行干燥、粉碎,即可得到碳酸钡成品。该方法工艺简单、成本低,因而被大多数厂家采用。
- ②复分解法
- 由硫化钡与碳酸铵进行复分解反应,反应如下:
- BaS+(NH4)2CO3=BaCO3+(NH4)2S
- 或用氯化钡与碳酸钾反应,反应如下:
- BaCl2+K2CO3=BaCO3+2KCl
- 反应所得的产物再经洗涤、过滤、干燥等,即可以得到碳酸钡成品。
- ③毒重石化法
- 将毒重石矿粉与铵盐反应生成可溶性钡盐,同时将碳酸铵回收使用,可溶性钡盐加入碳酸铵沉淀出精制碳酸钡,经过滤、干燥后制成成品。此外,得到的母液可回收循环使用。反应如下:
- BaCO3+2HCl=BaCl2+H2O+CO2
- BaCl2+2NH4OH=Ba(OH)2+2NH4Cl
- Ba(OH)2+CO2=BaCO3+H2O
- (2)钛酸钡的制取方法
- ①固相法
- 通过煅烧碳酸钡和二氧化钛可制得钛酸钡,其中可掺杂任意其他材料。反应如下:
- TiO2 + BaCO3 = BaTiO3 + CO2↑
- ②共沉淀法
- 将氯化钡和四氯化钛按等物质混合溶解,加热至70°C,然后滴入草酸,得到水合草酸钛酰钡[BaTiO(C2O4)2•4H2O]沉淀,经洗涤、干燥,再进行热解,最后得到钛酸钡。反应如下:
- BaCl2 + TiCl4 + 2H2C2O4 + 5H2O = BaTiO(C2O4)2•4H2O↓ + 6HCl
- BaTiO(C2O4)2•4H2O = BaTiO3 + 2CO2↑ + 2CO↑ + 4H2O
- 偏钛酸经打浆后加入氯化钡溶液,然后在搅拌下加入碳酸铵,生成碳酸钡和偏钛酸共沉淀,煅烧后得产品。反应如下:
- BaCl2 + (NH4)2CO3 = BaCO3 + 2NH4Cl
- H2TiO3 + BaCO3 = BaTiO3 + CO2↑ + H2O
- (3)氯化钡的制取方法
- 氯化钡的生产工艺按方法或原料的不同,主要有盐酸法、碳酸钡法、氯化钙法和氯化镁法。
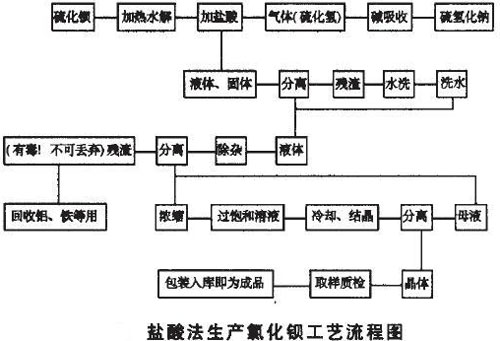
- ①盐酸法。用盐酸处理硫化钡,主要反应为:
- BaS+2HCI=BaCl2+H2S↑+Q
- ②碳酸钡法。以毒重石(碳酸钡)为原料制得,主要反应有:
- BaCO3+2HCI=BaCl2+CO2↑+H2O
- ③碳化法

- ④氯化钙法。用碳还原重晶石与氯化钙的混合物。
- 此外,还有氯化镁法。用氯化镁处理硫化钡制得。
-
-
介绍
-
历史发展
-
资源分布
-
应用
-
生产工艺
-
健康影响
-
环境影响
-
行业标准
-
名企
-
推荐
-
化合物
-
关于我们
联系我们
意见反馈
- 本站为公益性网站,旨在传播金属行业知识,为用户提供参考、借鉴和交流之用。知识内容整理秉承“新、全、专”原则,尽量为用户提供最可靠的知识信息。内容如有侵权请及时联系我们删除。







